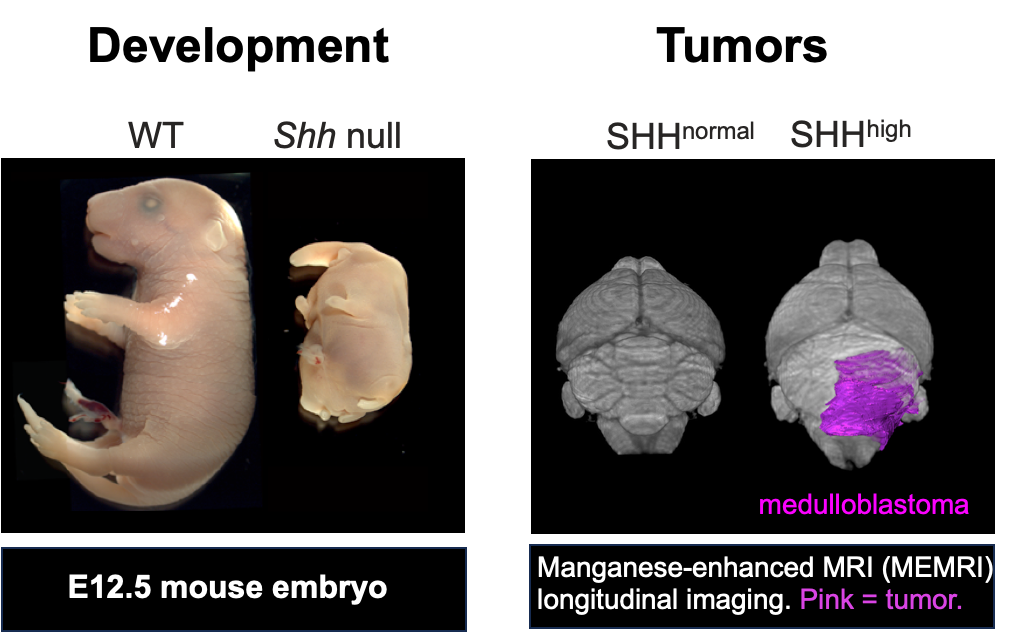
HH通路在胚胎发育和器官稳态中发挥重要作用,过度激活通路引起肿瘤。左图,野生型和Shh突变小鼠胚胎;右图,SHH髓母细胞瘤。




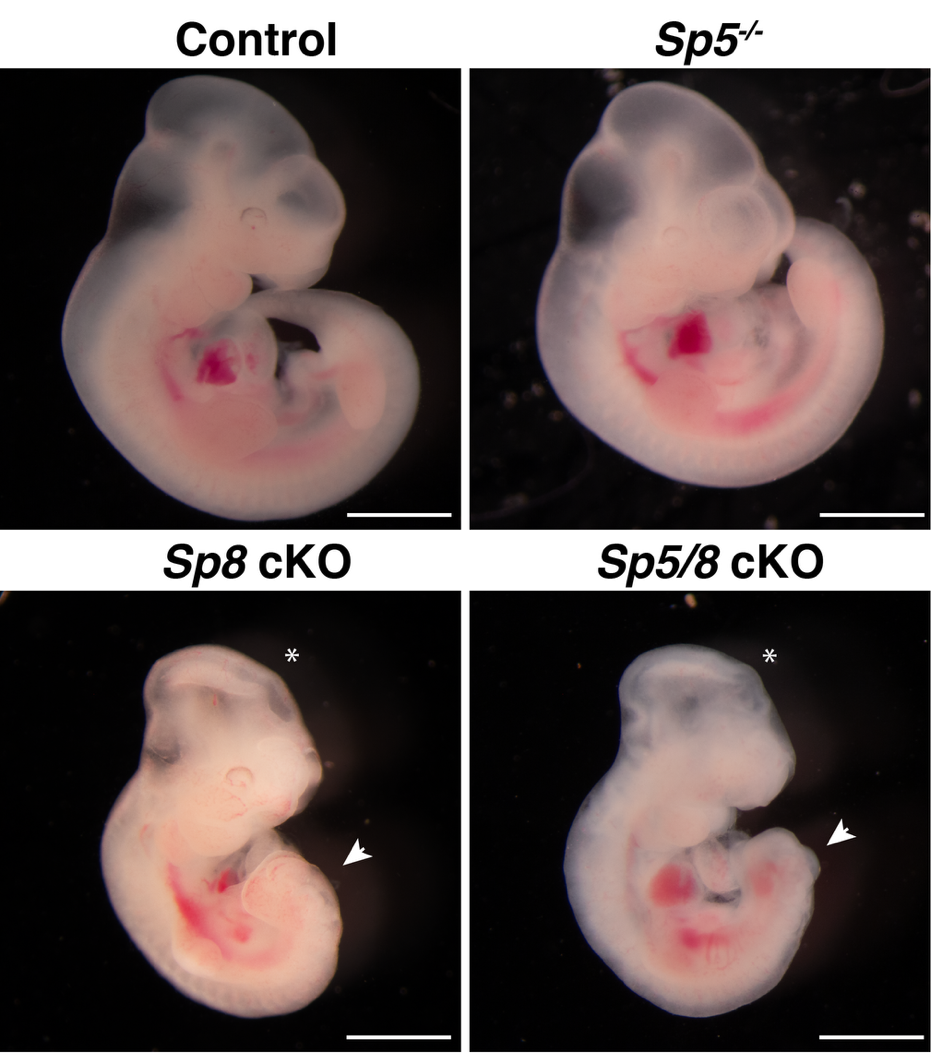
1. 发现SP5和SP8转录因子是原生纤毛形成的“总开关”(Science,2025)
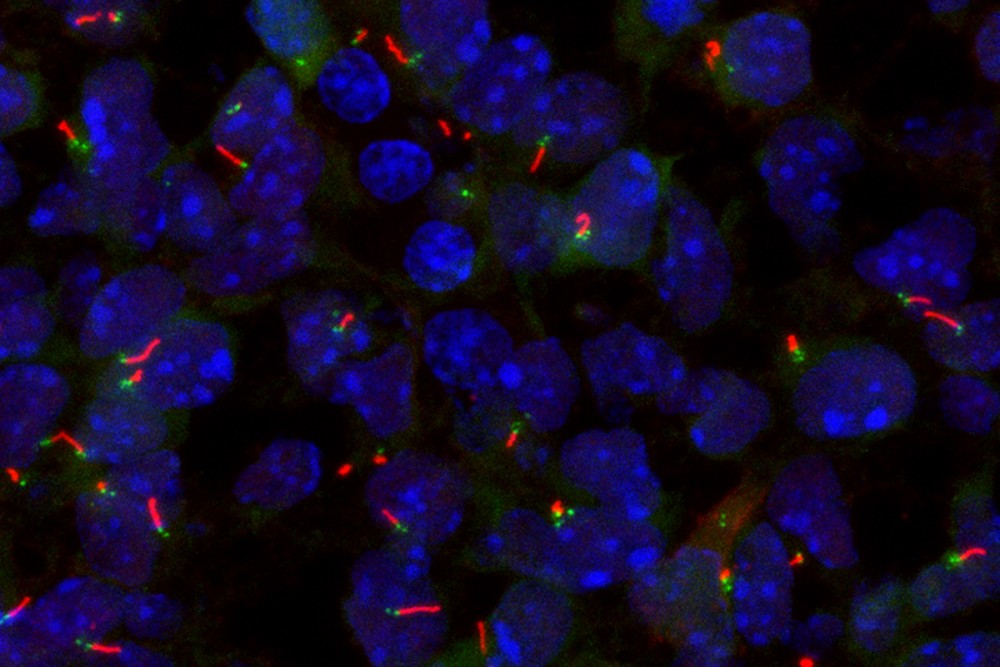
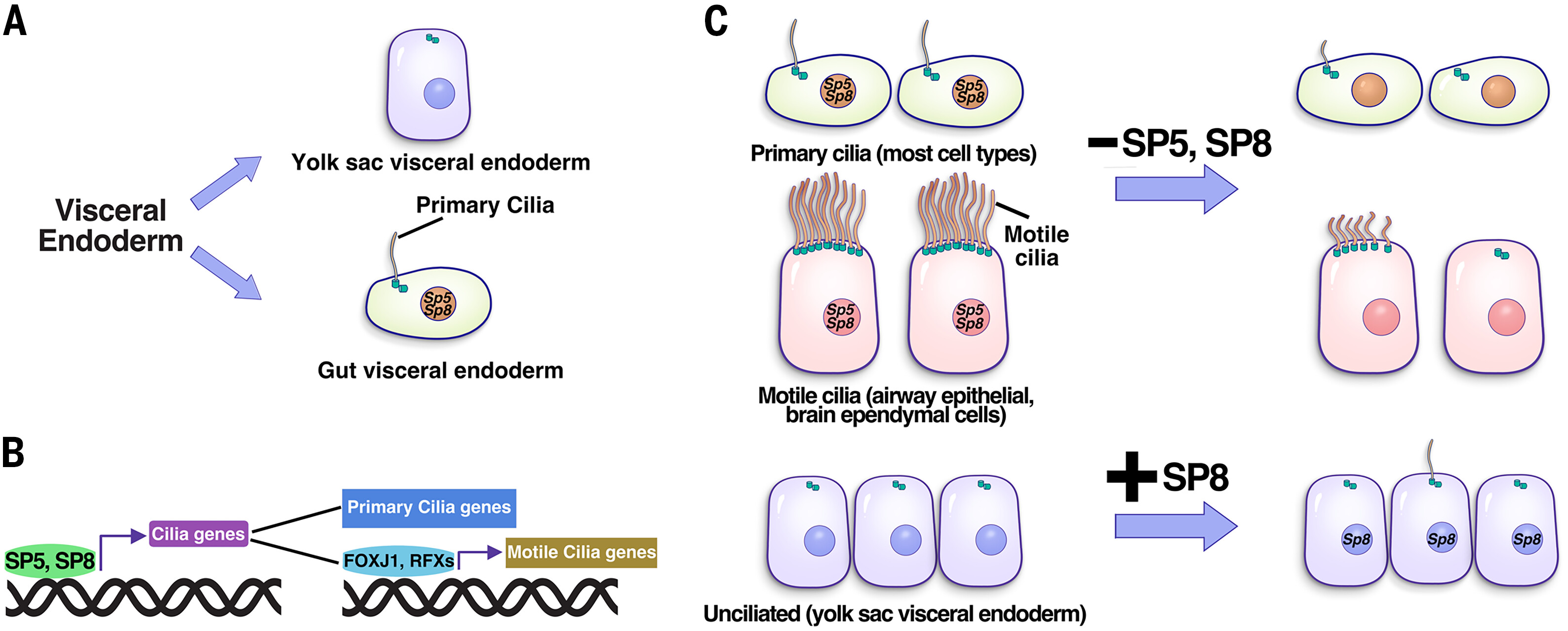
实验室发现了SP5和SP8作为纤毛形成的关键转录调控因子,首次证明了SP5和SP8直接结合并激活多个纤毛基因的表达,包括Foxj1和RFX家族转录因子。由SP5和SP8介导的转录调控网络是纤毛形成所必需的,并且SP8异位表达足以驱动纤毛的形成。

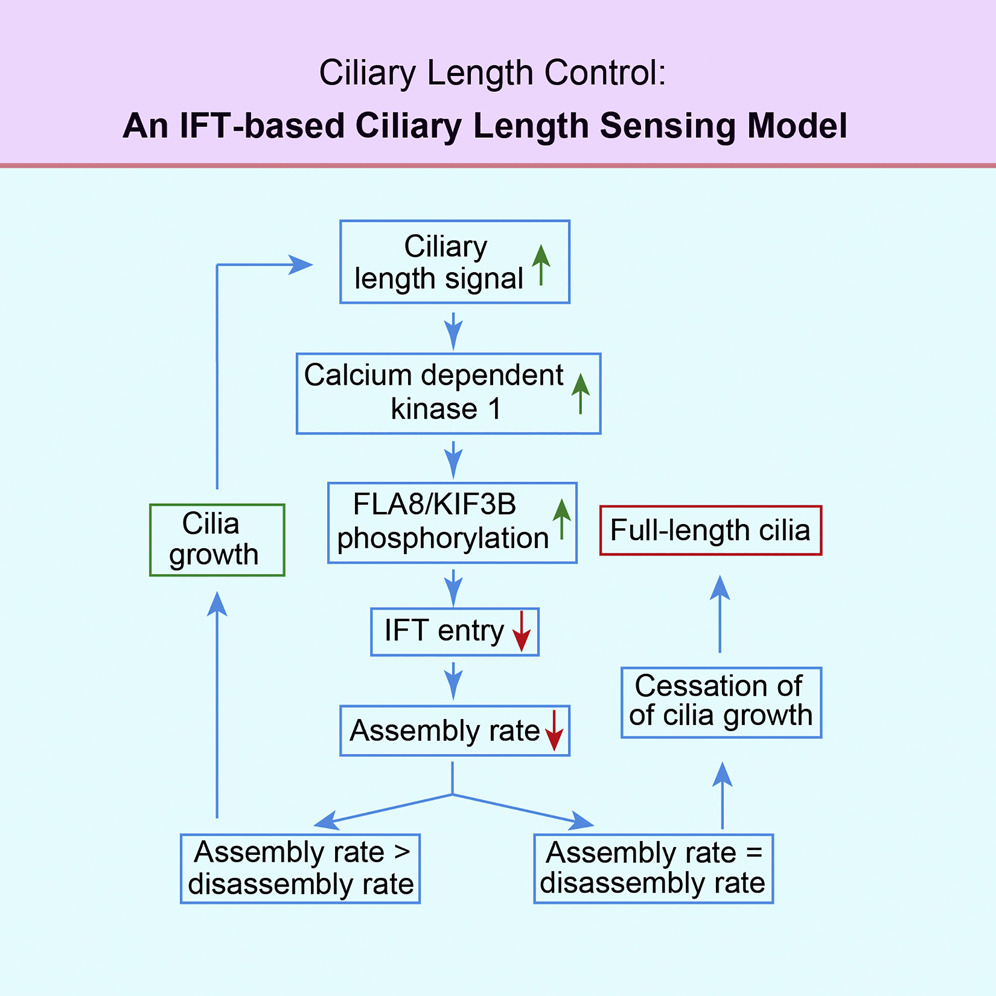
2. 阐明马达蛋白磷酸化调控机制,提出纤毛长度调控模型(Current Biology, 2018; Developmental Cell, 2014a; Developmental Cell, 2014b)
利用莱茵衣藻和小鼠模型,实验室的研究揭示了纤毛装配和内鞭毛运输(IFT)的分子机制,包括通过磷酸化KIF3B的S663位点对其的调控。实验室还提出了通过IFT负载速率控制纤毛长度的模型。