2026年4月16日,北京大学定量生物学中心的汤超团队和首都医学科学创新中心的任会霞团队在Cell Systems杂志发表了题为“Pancreatic islet oscillation rhythmicity arises from δ and α cell interactions”的研究论文。该研究发现胰岛中占比少的δ细胞与α细胞,是调控胰岛β细胞节律的核心网络;团队结合微流控技术、数学建模与活体成像,系统阐明了δ-α细胞旁分泌互作调控β细胞,形成三种钙振荡模式的核心机理,并揭示了胰岛通过振荡模式编码血糖浓度的全新机制。

技术创新:搭建高通量胰岛功能 - 结构关联成像体系
胰岛直径分布于50-200μm之间,为实现不同尺寸胰岛的高通量稳定灌流与同步成像,研究团队自主研发微流控芯片(专利号ZL 2024 1 0739918.1),可同步完成8个胰岛的功能活动成像;同时构建α细胞红色荧光标记、全胰岛钙信号绿色荧光标记的转基因小鼠模型,结合双光子显微镜实现胰岛功能活动与三维结构的精准关联分析。基于该技术体系,研究团队发现:同一胰岛在重复高糖刺激下,钙振荡模式高度稳定可重复,证实胰岛振荡模式是其自身固有的生理属性,为后续机制研究奠定了基础。
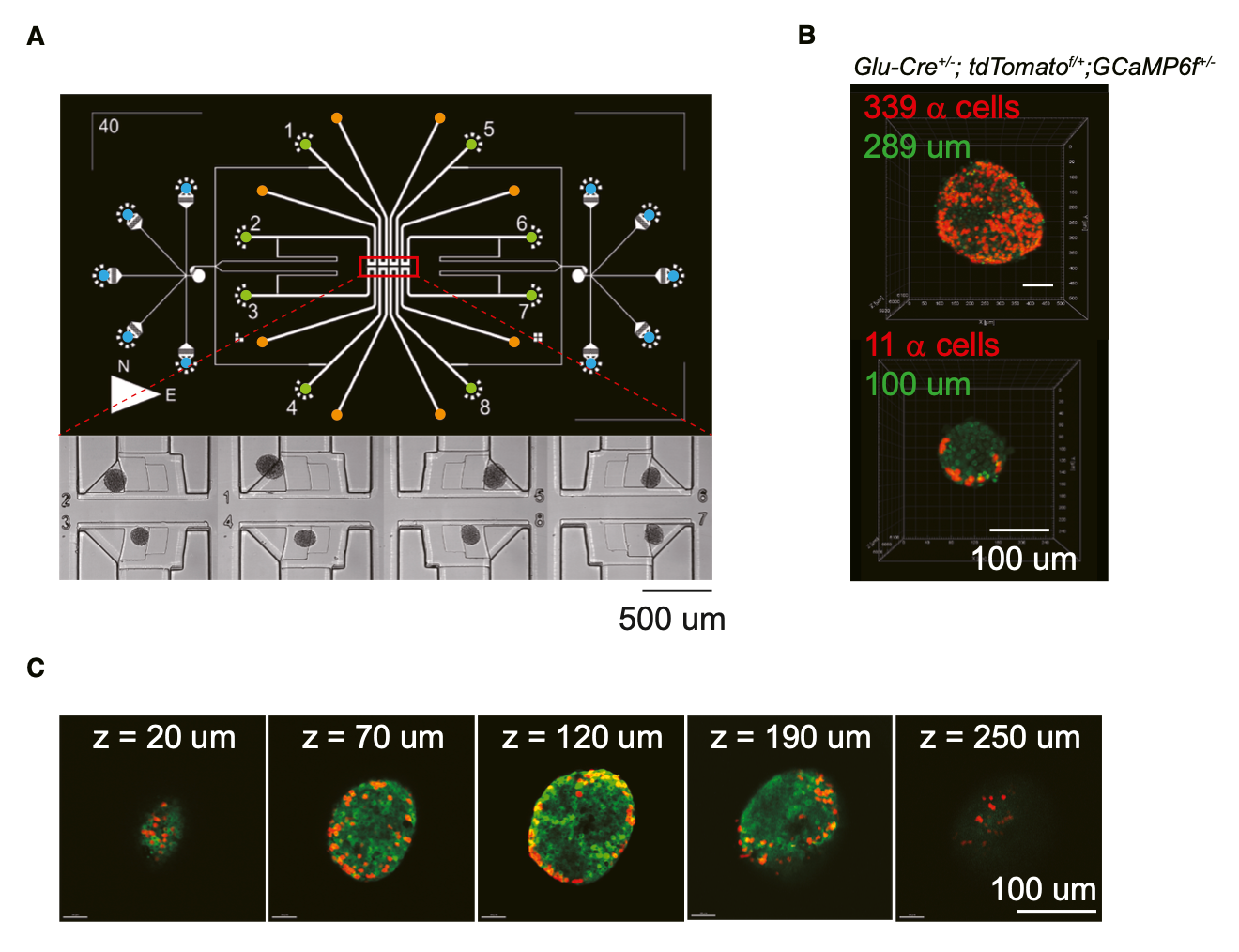
图1:为探索葡萄糖刺激胰岛钙活动与结构关系,研究团队设计了集成微流控芯片,实现8个胰岛同步活动成像,功能成像后通过双光子显微镜成像胰岛结构。
1.胰岛振荡模式异质性由α细胞数量决定
高糖刺激实验表明,胰岛钙振荡模式与α细胞数量呈定量依赖关系(图2):当胰岛内α细胞数量多于40个时,呈现快速振荡;α细胞数量少于40个时,呈现慢速振荡。外源干预实验进一步验证调控:补充胰高血糖素可使所有胰岛转为快速振荡,且不再依赖α细胞数量;补充生长抑素则可诱导振荡模式转为慢速,且振荡仍然依赖α细胞数量, 1μM生长抑素可将快速振荡的α细胞数量阈值从40个提升至100个。该结果明确,胰岛振荡模式受δ细胞(分泌生长抑素)与α细胞(分泌胰高血糖素)的旁分泌信号协同调控。
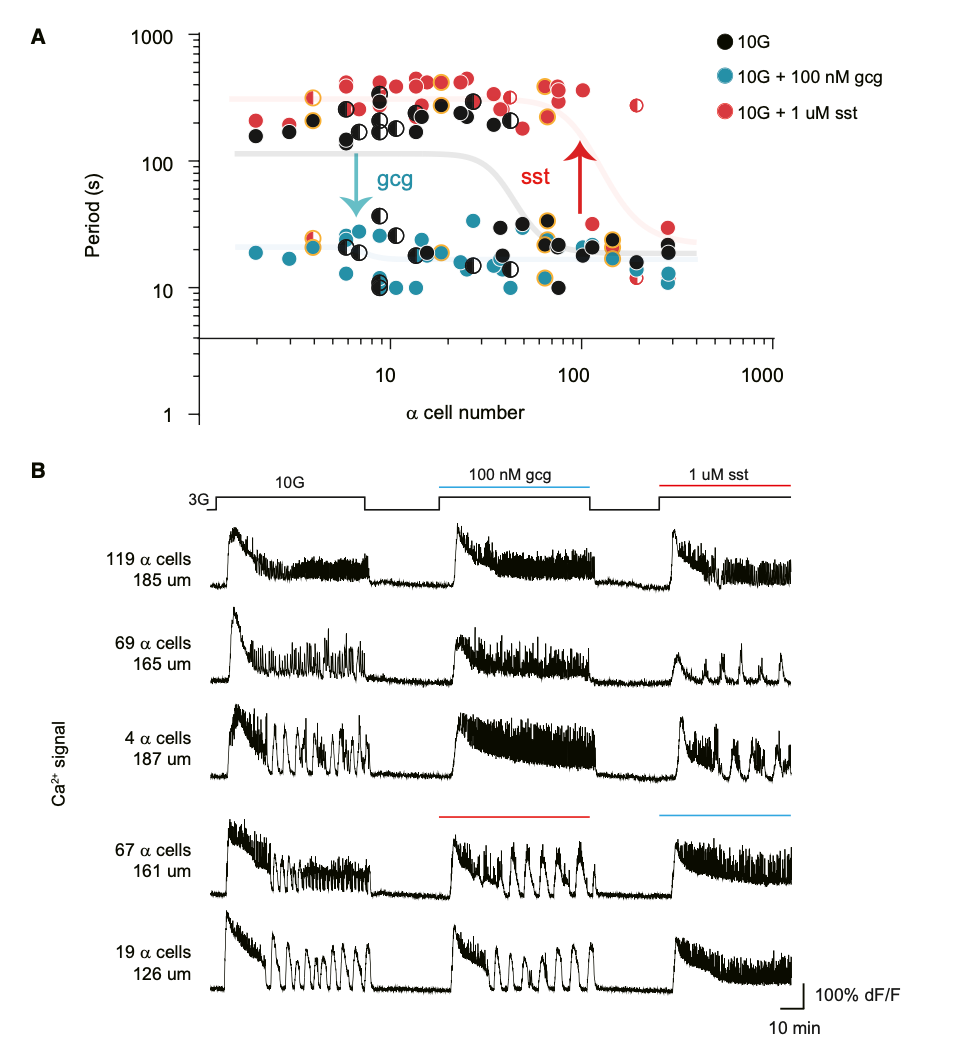
图2:胰岛震荡模式依赖于胰岛α细胞数量,且可被外源胰高血糖素及生长抑素调控。
2.药理学、光遗传抑制δ细胞可逆的转换胰岛震荡模式
δ细胞仅占胰岛细胞总数的5%,为验证少量细胞的内源激素的调控作用,团队开展药理学与光遗传扰动实验(图3):通过Sstr2受体拮抗剂CYN解除δ细胞对α细胞的抑制,内源胰高血糖素释放可使慢速振荡可逆转为快速振荡,洗脱药物后振荡模式恢复;光遗传学抑制δ细胞可实现相同的模式转换,且该过程在单个胰岛中可重复发生。以上结果表明,占比较少的δ细胞与α细胞的内源激素分泌在胰岛节律调控中发挥着关键作用:α细胞激活主导快速振荡,δ细胞激活主导慢速振荡,少数δ-α细胞的内源激素互作,是胰岛节律调控的核心驱动力。
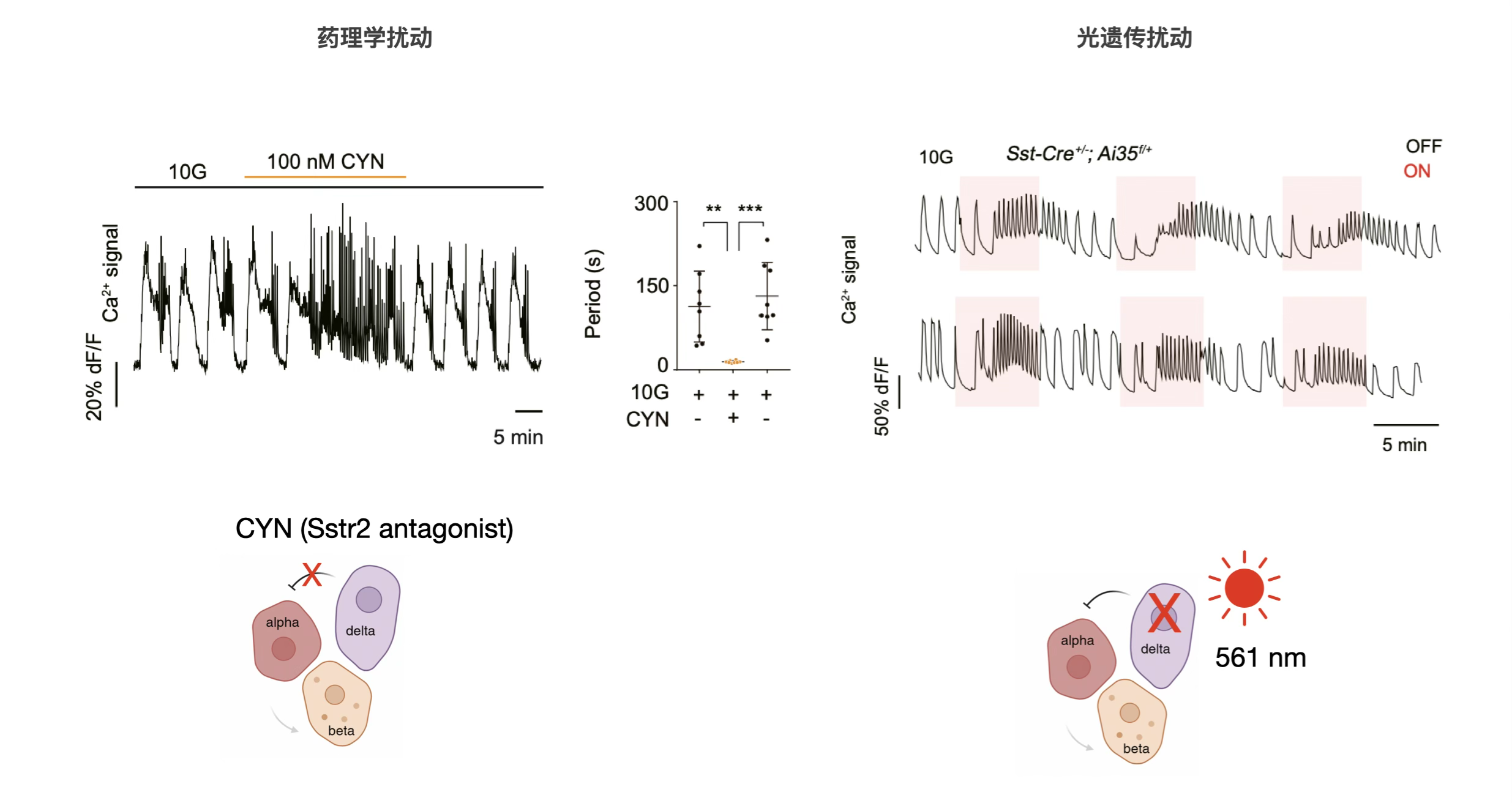
图3:药理学及光遗传扰动δ细胞可逆的转变胰岛震荡模式。
3.快速-混合-慢速震荡模式是δ-α细胞调控的三个连续生理状态
为了定量研究胰岛δ细胞与α细胞如何控制三种钙震荡模式,研究团队在不同α细胞数量的胰岛中连续升高生长抑素浓度(δ细胞分泌)。发现随着生长抑素浓度升高,胰岛依次从快速振荡→混合振荡→慢速振荡(图4)。有趣的是,若将α细胞数量连续排列,也有同样规律:α细胞数量最多的胰岛呈现快速震荡,数量最少的胰岛呈现慢速震荡,数量居中的胰岛呈现混合震荡。以上结果表明:快速、混合、慢速振荡是胰岛的三个连续生理状态,混合振荡为快慢振荡之间的过渡态,而δ细胞与α细胞的旁分泌作用强度,是决定振荡模式的核心参数。
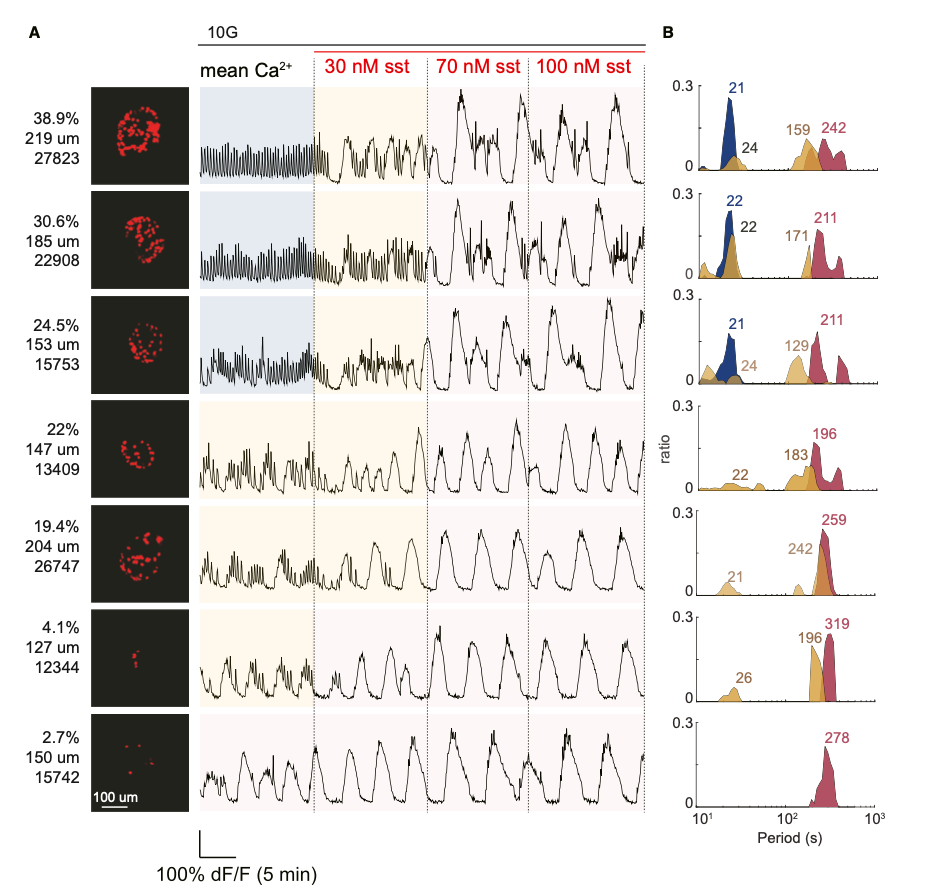
图4:快速-混合-震荡模式是δ细胞与α细胞介导的三个连续态,其中混合模式是介于快速与慢速震荡的过渡态。
4.数学模型揭示三种振荡模式转变为Hopf分岔相变
为定量阐释δ-α细胞的调控规律,团队将胰岛简化为α、β、δ细胞耦合的振荡器系统,以α→β细胞刺激作用、δ→α细胞抑制作用为核心参数构建数学模型(图5)。该模型可精准复现三种钙振荡模式,揭示模式转换的核心逻辑:慢速振荡对应α→β刺激弱,快速振荡对应刺激强,混合振荡为强弱刺激的极限环状态。分岔相图分析进一步明确,胰岛三种振荡模式的转换是Hopf分岔相变过程,为胰岛节律调控提供了定量生物学理论支撑。
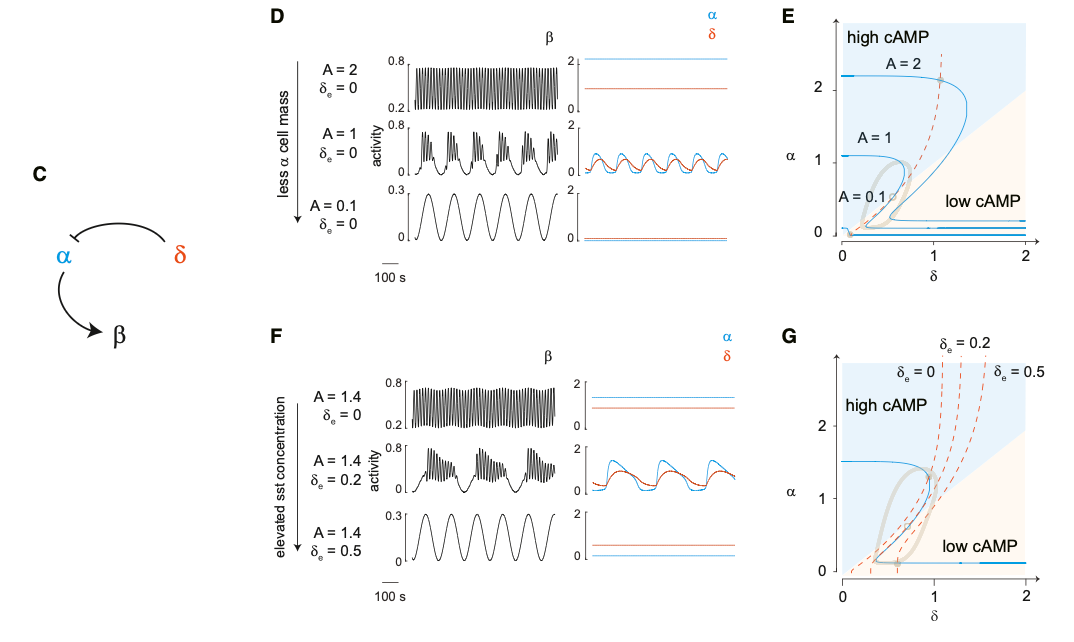
图5:数学模型复线δ细胞与α细胞介导的三个连续态快速-混合-慢速震荡模式是Hopf相变。
5.在体胰岛通过振荡模式精准编码血糖浓度
基于体内细胞激活特性(α细胞响应基础葡萄糖、δ细胞响应高糖),团队验证胰岛振荡模式是否作为在体血糖编码机制。结果显示:空腹血糖5-7mM时,胰岛呈快速振荡(图6);血糖升高至7-20mM时,转为慢速振荡;血糖恢复基础水平后,振荡模式同步复原。该结果表明,胰岛通过δ-α细胞调控的钙振荡模式,实现对血糖浓度的精准编码,提出机体血糖感知编码的新机制。
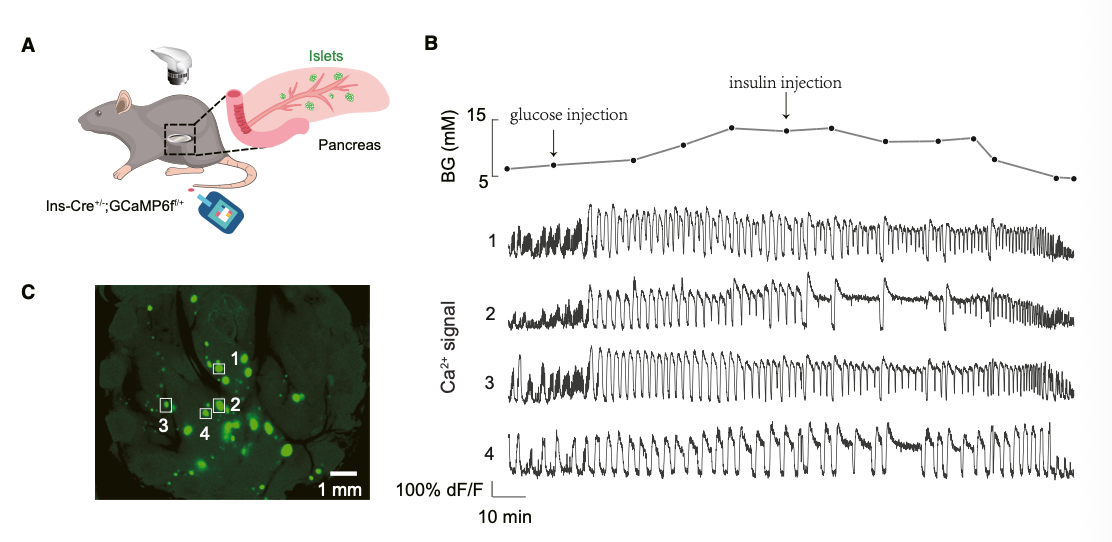
图6:在体胰岛通过震荡模式编码感受血糖浓度。
总结
本研究补充了传统胰岛功能研究的β细胞中心认知,明确δ、α细胞是胰岛节律调控的核心网络:α细胞分泌的胰高血糖素驱动快速钙振荡,δ细胞分泌的生长抑素维持慢速钙振荡,二者互作决定胰岛振荡模式。研究建立了胰岛功能定量研究的数学模型,在活体水平揭示了胰岛节律编码血糖的全新机制,为理解血糖稳态维持提供了新视角。
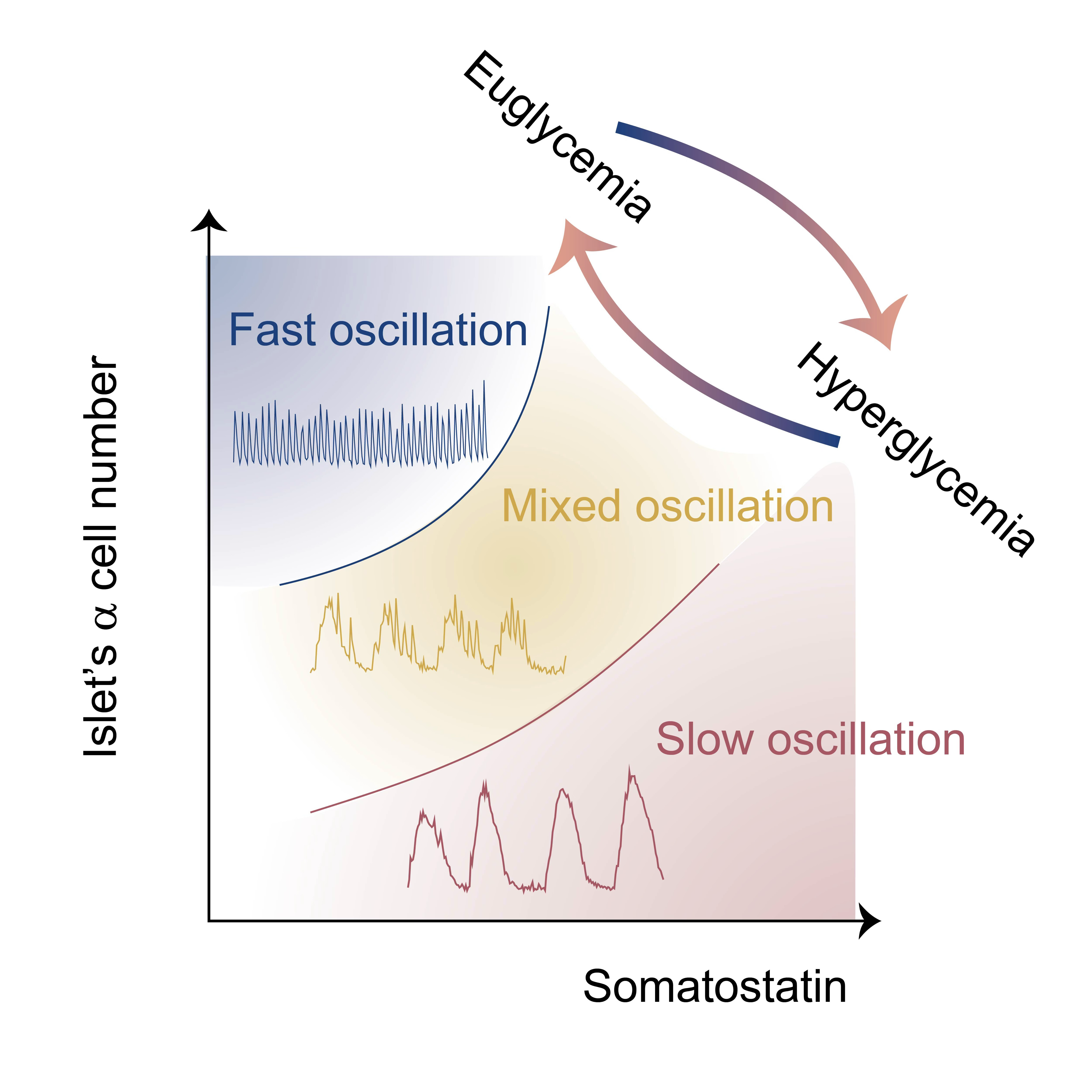
近日,任会霞课题组在Cell Systems同期的“Glycemia shifts pancreatic islet rhythmicity by influencing interactions between δ cells and α cells”研究论文,进一步报道了健康胰岛群体在体节律的血糖编码机制,以及该节律模式在糖尿病状态下的紊乱特征。
该研究得到了国家自然科学基金、首都医学科学创新中心等多个项目和平台的支持。
首都医学科学创新中心任会霞、北京大学黎彦君、谢北辰、彭晓红与首都医学科学创新中心付振超作为共同第一作者,北京大学汤超研究员、首都医学科学创新中心任会霞研究员为论文共同通讯作者。
原文链接:Pancreatic islet oscillation rhythmicity arises from δ and α cell interactions: Cell Systems
汤超
中国科学院院士
北大-清华生命科学联合中心PI
邮箱:tangc@pku.edu.cn
研究领域:生物网络中的功能与拓扑结构的关系;细胞周期调控的系统设计原理;细胞是如何做各种决定的;发育、细胞分化及重编程;微生物的生长、代谢及对环境的响应;器官中的细胞震荡机理与调控;信息论与人工智能在生物系统中的应用。
研究兴趣:我们应用和发展定量的方法和工具,有机地结合理论、计算和实验来提出和解决关键生物学问题。以求通过对生物系统的定量的交叉的研究,来发现生物世界中的基本定量规律和普适性原理,寻找生命的数学语言和生命的物理。
任会霞
首都医学科学创新中心青年研究员
邮箱:renhuixia@cimrbj.ac.cn
研究领域:实验室致力于胰岛结构与生理功能研究,关注 “在体胰岛群体节律活动如何编码并调控血糖状态转变,以应对高血糖与低血糖”。通过建立 “在体大视场多胰岛实时成像 + 连续血糖监测 + 微流控与分泌探针 + 数学建模” 的交叉技术体系,探究代谢压力异常引发的糖尿病、肥胖等代谢性疾病机制的理解,为相关治疗策略提供新的理论依据与思路。