血糖稳态是机体维持正常代谢的基础,而胰腺胰岛作为调控血糖的核心功能单元,其功能高度依赖于内部细胞间的通讯与群体协作。胰岛主要由约80%的β细胞(分泌胰岛素)、15%的α细胞(分泌胰高血糖素)和5%的δ细胞(分泌生长抑素)组成,这些细胞紧密排列,形成复杂的旁分泌调控网络。在功能层面,胰岛呈现节律性钙振荡,驱动激素的脉冲式释放。
近年研究已证实,胰岛的节律性振荡对血糖控制至关重要。然而,一个核心问题长期未解:人体胰腺中分布着上百万个胰岛(小鼠约数千个),它们如何像一支交响乐团般协同“演奏”,共同维持血糖稳定?目前的研究局限于单个胰岛或离体组织,缺乏在活体水平同步观测数十甚至上百个胰岛动态行为的技术手段。因此,在血糖从高到正常、从稳定到波动的变化过程中,成百上千个胰岛如何协同“换挡”,感知并编码血糖状态,仍有待揭示。

近日,首都医学科学创新中心医学生理学研究所任会霞研究员团队联合中国科学院杭州医学研究所、北京大学、深圳大学等机构,在Cell Systems上发表题为“Glycemia shifts pancreatic islet rhythmicity by influencing interactions between δ cells and α cells”的研究。该研究通过构建胰岛特异性荧光标记小鼠模型,结合连续血糖监测的大视场成像系统,首次实现了对活体小鼠胰腺内20–100个胰岛长达4小时以上的钙活动动态观测,发现机体血糖水平由胰岛群体钙振荡节律编码,其节律核心的调控网络由胰岛内少数细胞类型δ及α细胞构成(图1)。
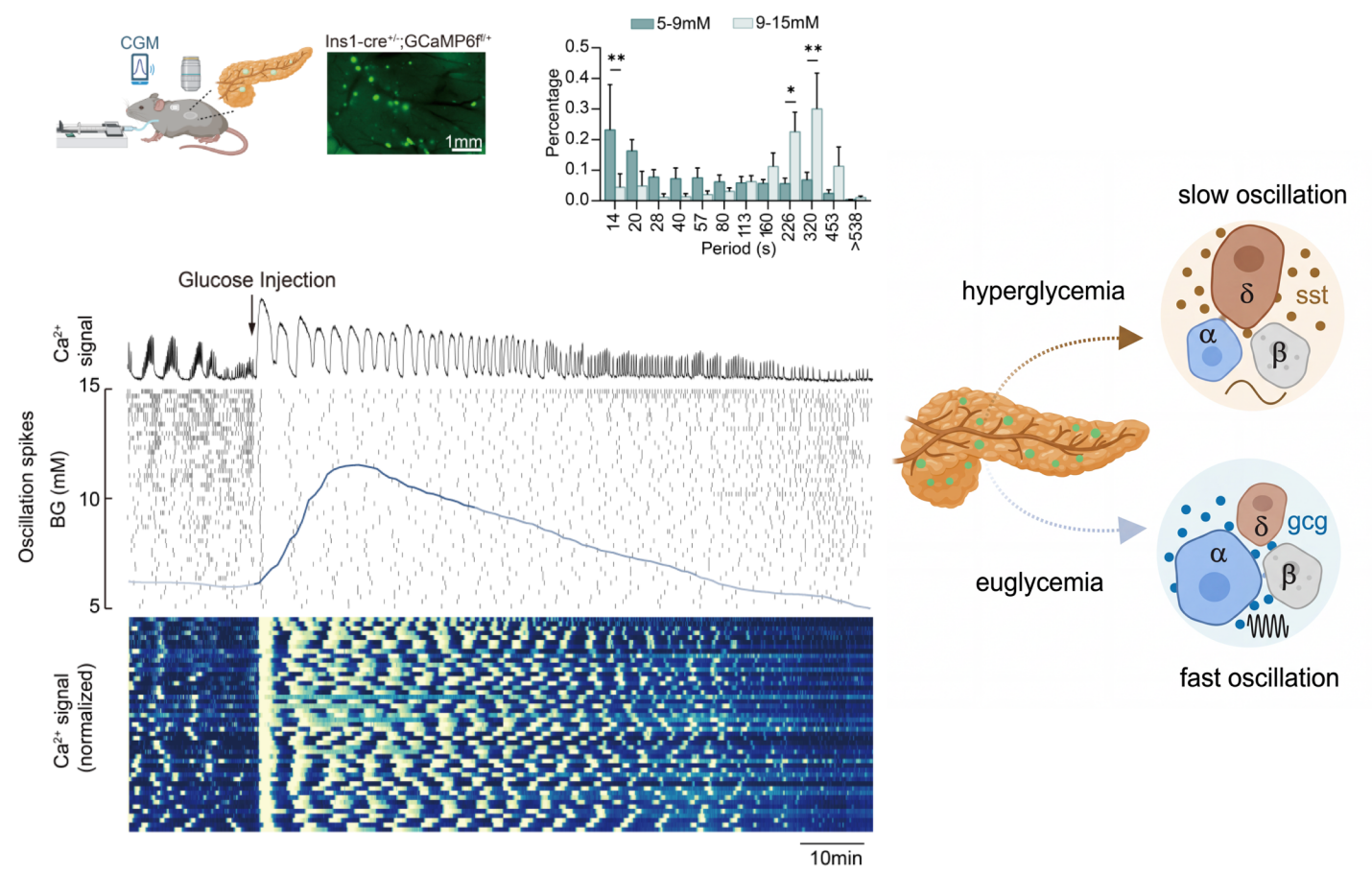
图1. 为探索血糖如何调节胰岛群体活动,研究团队在活体小鼠中实现了20–100个胰岛的同步钙成像观测,发现胰岛钙振荡节律会随血糖水平发生精准的协同性慢-快转变:当血糖从高血糖状态回落至正常血糖水平时,胰岛钙振荡周期会从226–320秒的慢周期,同步切换为14–20秒的快周期,这一转变是健康胰岛适应血糖变化、维持血糖稳态的重要特征。
视频:胰岛在机体血糖变化过程中的慢-快节律转换。图中数字表示血糖水平,荧光显示胰岛胞内钙浓度。
基于这一从高血糖恢复至正常血糖过程中的“慢-快节律转换”(Hyperglycemia to euglycemia induced slow to fast oscillation, HESF)现象,研究团队进一步设计实验,探索其调控机制及在疾病模型中的变化:
(1)多层级模型揭示:血糖依赖的节律转变离不开胰岛内“对话”
为验证该现象的调控基础,研究团队构建了“在体血糖钳制 - 胰腺组织切片 - 分散单细胞” 的多层级实验模型(图2)。结果显示,血糖依赖的节律转变在保留细胞间旁分泌信号的胰腺组织切片中依然存在,但在失去旁分泌交流的分散β细胞中完全消失。这明确了胰岛内细胞间旁分泌信号是HESF现象的核心调控基础,突破了以往仅关注β细胞自主节律的认知局限。
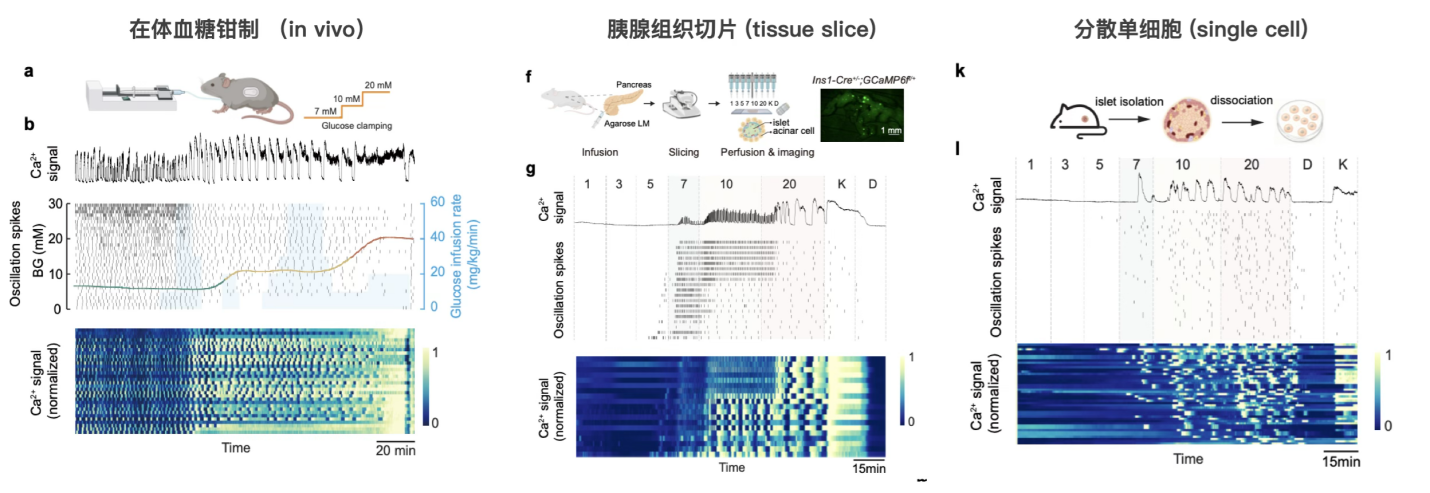
图2. “在体血糖钳制 - 胰腺组织切片 - 分散单细胞”的多层级实验模型。
(2)胰岛节律调控机制解析:δ细胞与α细胞相互作用主导胰岛节律调控
为探究胰岛节律的旁分泌调控机制,研究团队在体外分离胰岛中进行了高糖刺激实验(图3)。结果显示,在高糖环境下,胰岛呈现出两种内在的、可重复的钙振荡模式——快振荡与慢振荡,据此可将胰岛分为两类。进一步实验发现,添加外源性胰高血糖素(由α细胞分泌)后,无论原本是快振荡还是慢振荡的胰岛,均转变为快速振荡模式;而添加生长抑素(由δ细胞分泌)后,两类胰岛则均转变为慢速振荡模式。这一结果表明,δ细胞与α细胞的相互作用在胰岛节律调控中发挥着关键作用:α细胞的激活主导快振荡的发生,δ细胞的激活则主导慢振荡的维持。
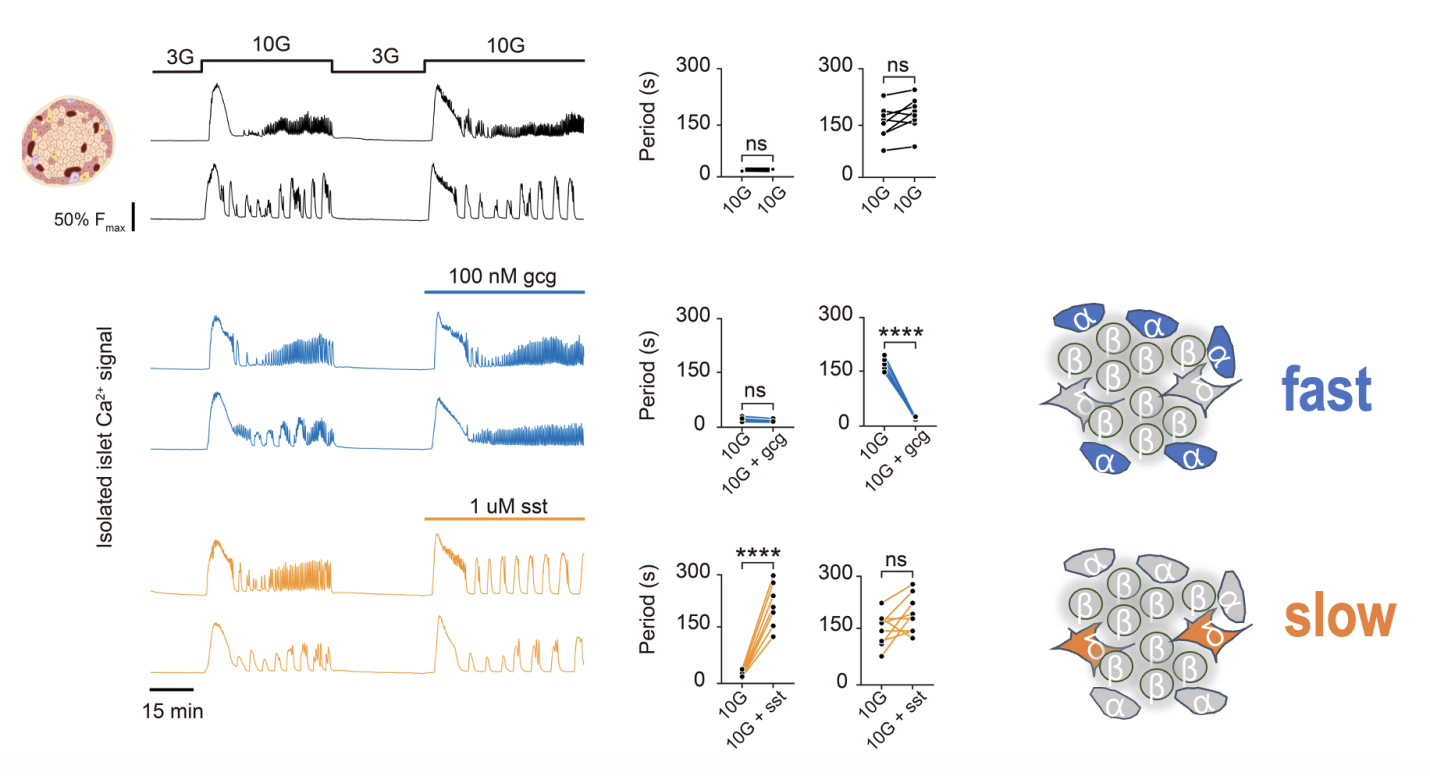
图3. 外源添加胰高血糖素及生长抑素改变离体胰岛振荡模式。
(3)血糖编码机制解析:δ-α细胞相互作用构成胰岛节律调控核心
那么,血糖水平是如何通过δ细胞与α细胞的相互作用实现节律编码的呢?以往研究已明确,α细胞对低血糖强响应,而δ细胞对高血糖强响应。基于此,研究团队提出如下调控模型:在高血糖状态下,δ细胞被激活并分泌生长抑素,进而抑制α细胞活性,使胰岛呈现慢钙振荡节律;当血糖恢复至正常水平时,δ细胞的抑制作用解除,α细胞被激活并分泌胰高血糖素,进而触发胰岛的快钙振荡节律。为进一步验证这一猜想,团队开展了受体阻断实验。结果显示,阻断δ细胞对α细胞的抑制,或激活相关信号通路,均可有效调控胰岛的钙振荡周期(图4)。这一系列实验证实,δ–α细胞相互作用是血糖状态编码胰岛节律的核心机制:α细胞的激活主导快振荡,δ细胞的激活主导慢振荡,二者通过旁分泌信号实现血糖水平的动态响应与节律转换。
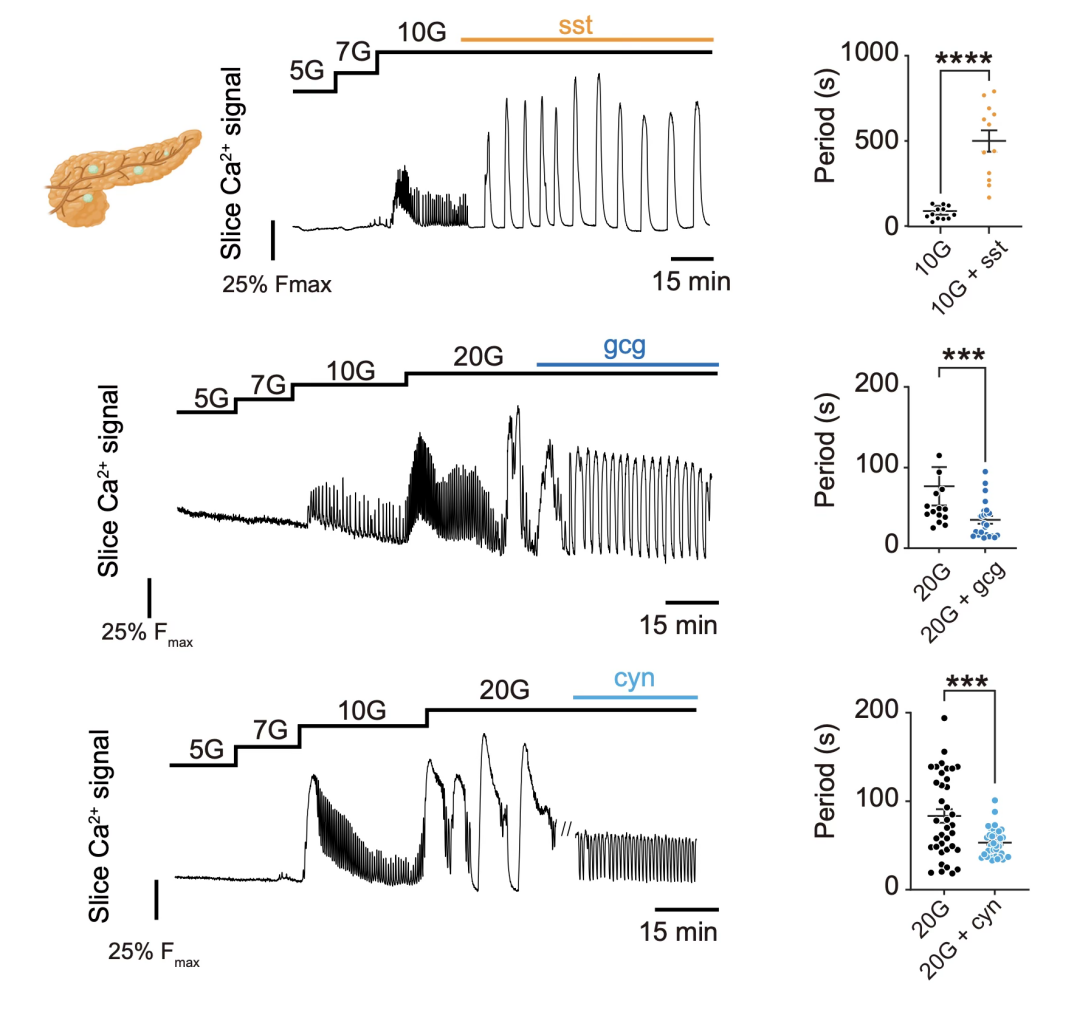
图4. 外源添加胰高血糖素及生长抑素改变组织切片中葡萄糖诱导的胰岛振荡模式。
(4)糖尿病中的关键缺陷:胰岛节律转变功能的丧失
为探究该调控机制与糖尿病的关联,研究团队利用肥胖糖尿病(ob/ob)小鼠模型开展验证实验(图5)。结果发现,糖尿病小鼠存在显著的血糖稳态失衡,其胰岛在体内外均完全丧失了HESF节律转变功能:不仅在正常血糖下无法产生快钙振荡,高血糖下的慢振荡也失去了血糖依赖性调控,同时胰岛对血糖变化的敏感性显著降低,具体表现为低葡萄糖水平下即出现异常激活、在高血糖下持续激活能力下降等特征。这一系列缺陷成为糖尿病小鼠血糖调控失常的重要原因。
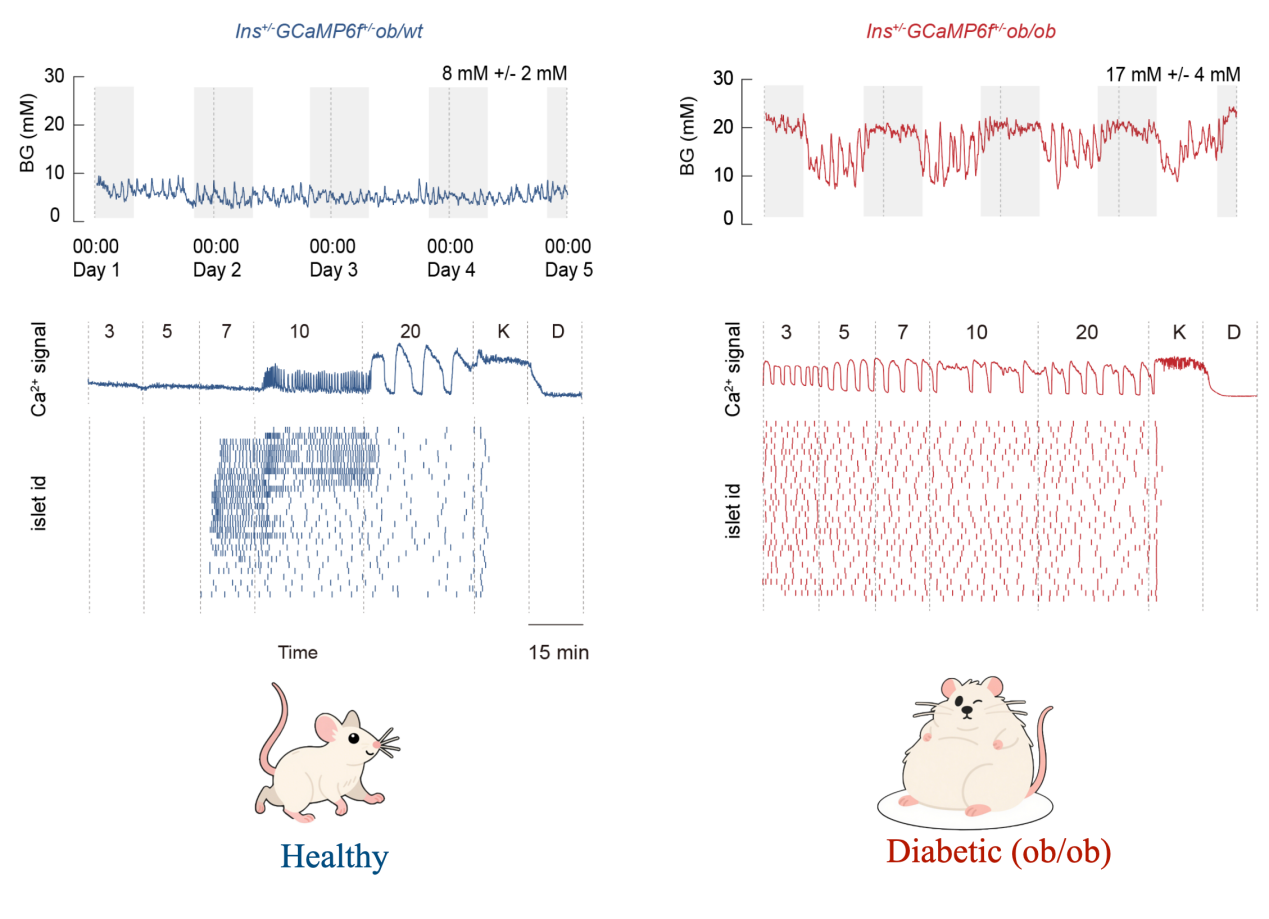
图5. 健康及糖尿病小鼠连续血糖监测(上)及葡萄糖刺激胰岛群体钙活动(下)。
(5)胰岛节律转变依赖于胰岛内GLP-1受体激活
机制上,研究发现胰岛快钙振荡的产生依赖于GLP-1受体(Glp1r)的内源性激活(图6),GLP-1受体激动剂司美格鲁肽可有效激活该通路,不仅能快速降低糖尿病小鼠的血糖水平,还能恢复其胰岛的HESF节律转变功能,使胰岛钙振荡模式恢复至接近正常小鼠的状态。
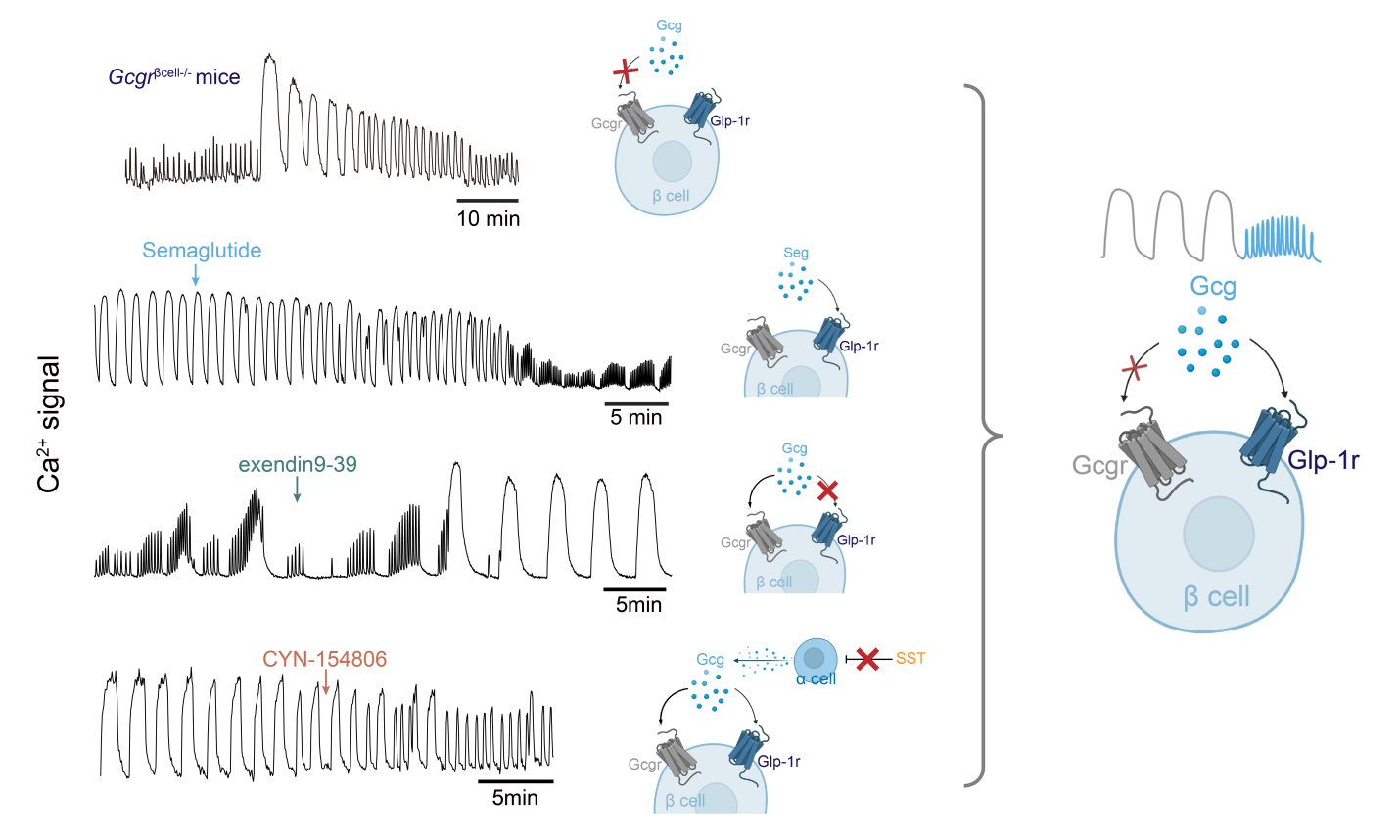
图6. 扰动GLP-1受体激活通路改变在体胰岛钙振荡模式。
总结
该研究在活体水平揭示了血糖调控胰岛节律的全新机制,明确了δ-α细胞相互作用介导的胰岛节律调控在高血糖编码中的核心作用,为理解血糖稳态的维持机制提供了新的视角。同时,研究证实糖尿病状态下胰岛节律转变功能的丧失是血糖调控失常的重要特征,而GLP-1受体激活可有效恢复该功能,这一发现为糖尿病的治疗提供了新的思路,也为后续开发靶向δ-α细胞相互作用的新型药物奠定了实验基础。
该研究得到了首都医学科学创新中心、国家自然科学基金、中国科学院杭州医学研究所等多个项目和平台的支持。

首都医学科学创新中心博士生邓雅文、博士后付振超与博士生王雪娇为论文共同第一作者,任会霞研究员、中国科学院杭州医学研究所杜媛媛研究员与深圳大学彭晓红研究员为论文共同通讯作者。
任会霞
首都医学科学创新中心青年研究员
邮箱:renhuixia@cimrbj.ac.cn
任会霞实验室长期致力于胰岛结构与生理功能研究,重点关注“在体胰岛群体节律活动如何编码并调控血糖状态转变,以应对高血糖与低血糖”。通过建立“在体大视场多胰岛实时成像 + 连续血糖监测 + 微流控与分泌探针 + 数学建模”的交叉技术体系,我们发现胰岛内δ细胞与α细胞构成了节律调控的核心网络,并在高糖条件下介导节律编码过程。未来,实验室将通过系统观察葡萄糖刺激下胰高血糖素、生长抑素、胰岛素等激素的释放模式,深化对代谢压力异常引发的糖尿病、肥胖等代谢性疾病机制的理解,为相关治疗策略提供新的理论依据与思路。