撰文|杨家俊(2024级博士研究生)
审核|李国民
2026年3月13日下午,应首都医学科学创新中心特聘研究员、肿瘤研究所所长李国民老师的邀请,清华大学李丕龙教授来访并作题为“Phase separation in transcriptional regulation”的学术报告。
李丕龙教授是全球“液-液相分离”(Liquid-Liquid Phase Separation, LLPS)领域最具代表性的先驱之一。2012年,他在Michael Rosen实验室从事博士后研究期间,开创性地证明了“多价相互作用”是驱动相分离的关键机制。这一工作成功将“相变”的物理概念引入生物学研究领域,为细胞内无膜细胞器的形成机制奠定了理论基础。近年来,李教授进一步揭示了相分离在染色质高级结构组织与基因转录调控中的重要功能,并致力于开发针对异常“致病性相分离凝聚体”的靶向干预手段,积极推动该领域的临床转化。
概要
细胞内无时无刻不在发生各种生化反应。相较于分子均匀散布在细胞内依靠分子间运动随机碰撞发生反应,真核细胞具有独特的方式使反应在空间和时间上都受到精确的调控。传统上,人们认为这种细胞内的空间组织主要依赖于具有膜结构的细胞器,例如细胞核、线粒体和内质网等。然而,近年来的研究发现,细胞内还存在大量没有膜结构的亚细胞结构(membraneless organelles),如核仁(图1)。这些结构通常通过生物分子相分离(biomolecular phase separation)形成。相分离是指蛋白质和核酸等生物大分子通过多价相互作用,从周围的细胞质或细胞核环境中分离出来,形成高浓度的凝聚体(condensates),这一过程类似于物理体系中的液-液相分离,例如油和水的分离。通过调节凝聚体的形成和解聚,细胞可以精细地调控所需生化反应发生的地点与时间。
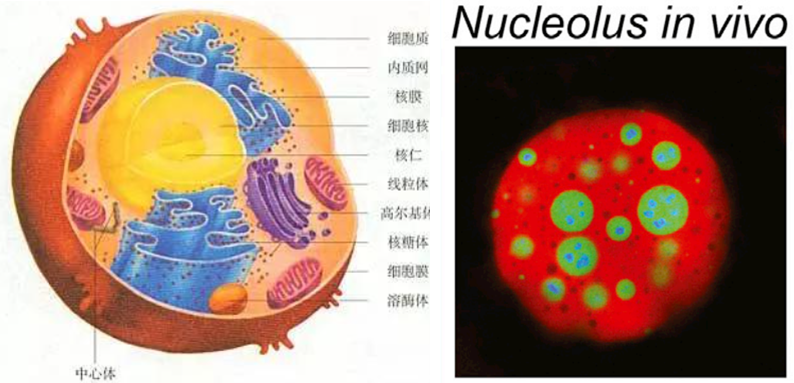
图1. 高中生物中提到的核仁是一种液-液相分离介导的凝聚体
报告中,李丕龙教授详细阐述了其团队通过结合生物物理学与细胞生物学方法,揭示了长链非编码RNA Xist与RNA结合蛋白HNRNPK能够通过液-液相分离(Liquid-Liquid Phase Separation, LLPS)在染色体表面形成动态凝聚体,从而限制Xist在染色体上的扩散,并富集染色质沉默因子,为X染色体失活的建立提供了一个相分离驱动的物理机制模型。
精彩回顾
雄性哺乳动物的性染色体为XY,而雌性哺乳动物的性染色体为XX。因此,理论上雌性X染色体编码蛋白表达量应该比雄性要多。但实际上,在早期胚胎发育中,细胞会随机且不可逆地沉默其中一条X染色体,关闭这条染色体上大范围基因的转录,这被称为X染色体失活(X-Chromosome Inactivation, XCI)。1991年,Carolyn J. Brown等人首次发现并鉴定了XCI的核心调控因子——XIST基因,其特异且排他性地仅在失活的X染色体上表达并停留,而在活跃的X染色体上保持沉默。但令人费解的是,带有与染色体相同负电荷的Xist RNA,是如何克服静电排斥并仅在特定X染色体上持续停留与蔓延的?其背后的物理机制长期未明。
HNRNPK自身可以形成凝聚体,且Xist可以促进其相分离
李丕龙教授团队首先确认了HNRNPK自身可以发生相分离。HNRNPK具有多个可以和RNA结合的结构域,包括3个KH结构域和1个RGG(精氨酸-甘氨酸-甘氨酸)结构域。其中RGG结构域属于一种内在无序序列(Intrinsically Disordered Region, IDR,图2A),可以通过多价相互作用在胞内或者体外自组装成液滴(图2B,C)。如果将介导该相互作用的关键氨基酸进行突变,该蛋白就会丧失形成液滴的能力。在该过程中,如果加入野生型的 RepB RNA-WT序列(Xist上负责定位失活X染色体的核心序列),可以显著促进HNRNPK 形成液滴;而如果加入无法与HNRNPK结合的突变型RepB-MU,则不能观察到该促进现象(图2D)。
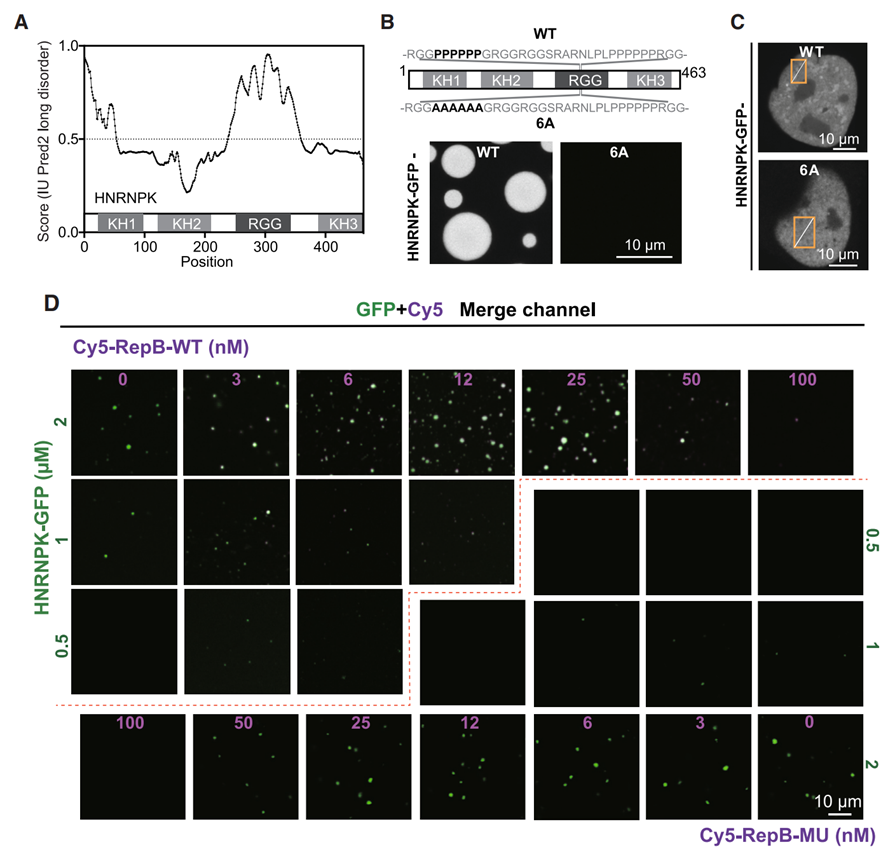
图2. HNRNPK可以形成液滴且Xist可以促进该过程
HNRNPK-RepB凝聚体可以招募、内化并富集其他XCI因子
研究团队进一步构建了多种XCI因子的融合蛋白,发现这些因子可以和HNRNPK-RepB一同形成共凝聚体(图3A)。同时,在已经形成HNRNPK-RepB凝聚体的体系中加入其他XCI因子时,这些游离蛋白会被逐渐招募、内化并富集进入已有的凝聚体内部(图3B)。通过光漂白恢复实验(FRAP)对这些液滴进行局部荧光淬灭,经过一段时间后发现淬灭区域的荧光逐渐恢复,直接证明了该凝聚体内部具有液体的动态流动性(图3C)。
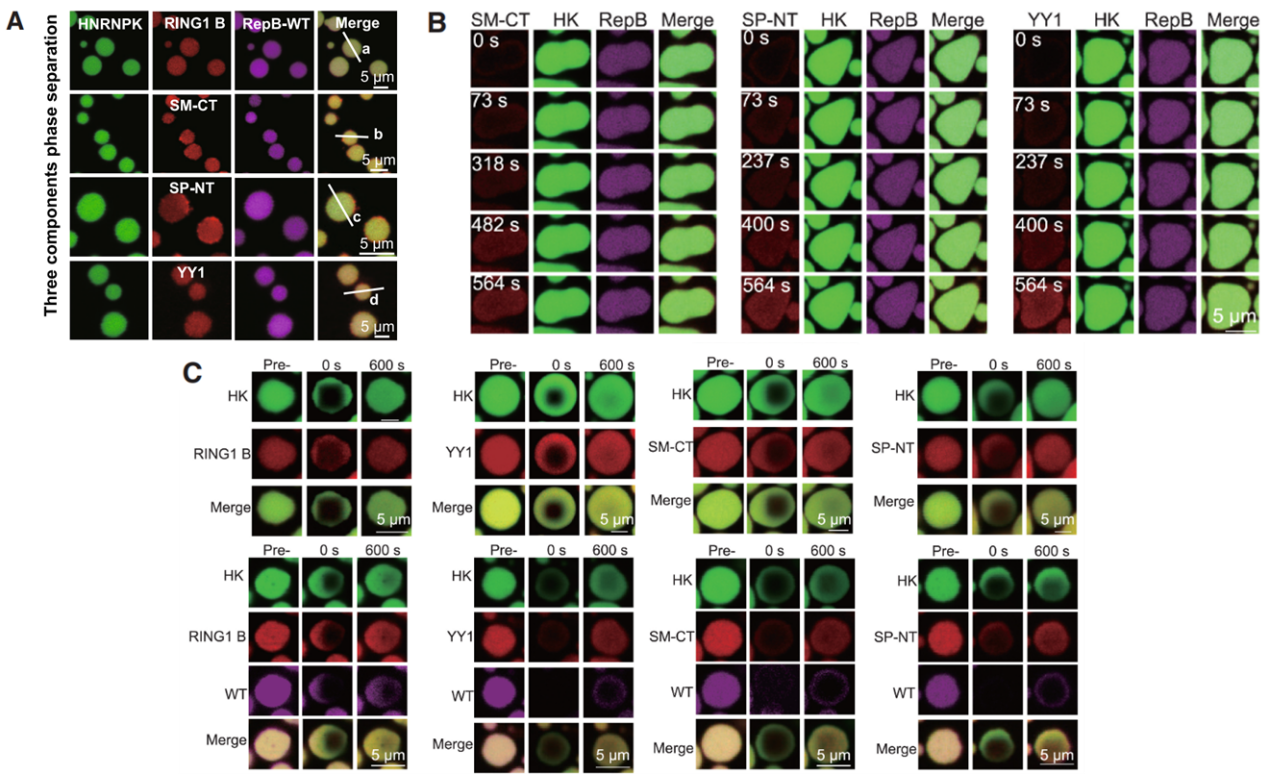
图3. HNRNPK-RepB凝聚体可以招募、内化并富集其他XCI因子一同形成凝聚体
RepB可以增加HNRNPK凝聚体的可变形性,且二者之间存在相互拉力
RepB和HNRNPK之间形成的凝聚体除了提高浓度,是否还存在其他生理功能? 李丕龙教授等人通过生物膜力探针技术(图4A)测定凝聚体的力学特性,发现结合RepB后,凝聚体的形变能力(Deformability)显著提升,变得更加“柔软”(图4B)。同时,利用该技术还发现,游离的RNA与HNRNPK凝聚体之间存在主动的物理拉力。结合这两点,RNA实际上极大提高了HNRNPK对染色质的润湿性能(Wetting properties,图4C)。基于此结果,他们提出:被招募的HNRNPK会与Xist形成柔软且具高润湿性的液滴,这种类似“液体薄膜”的特性,使得该凝聚体即使面对表面极不规则的染色质纤维,也能通过物理形变紧密贴合并发生顺式蔓延,从而发挥抑制转录的功能。
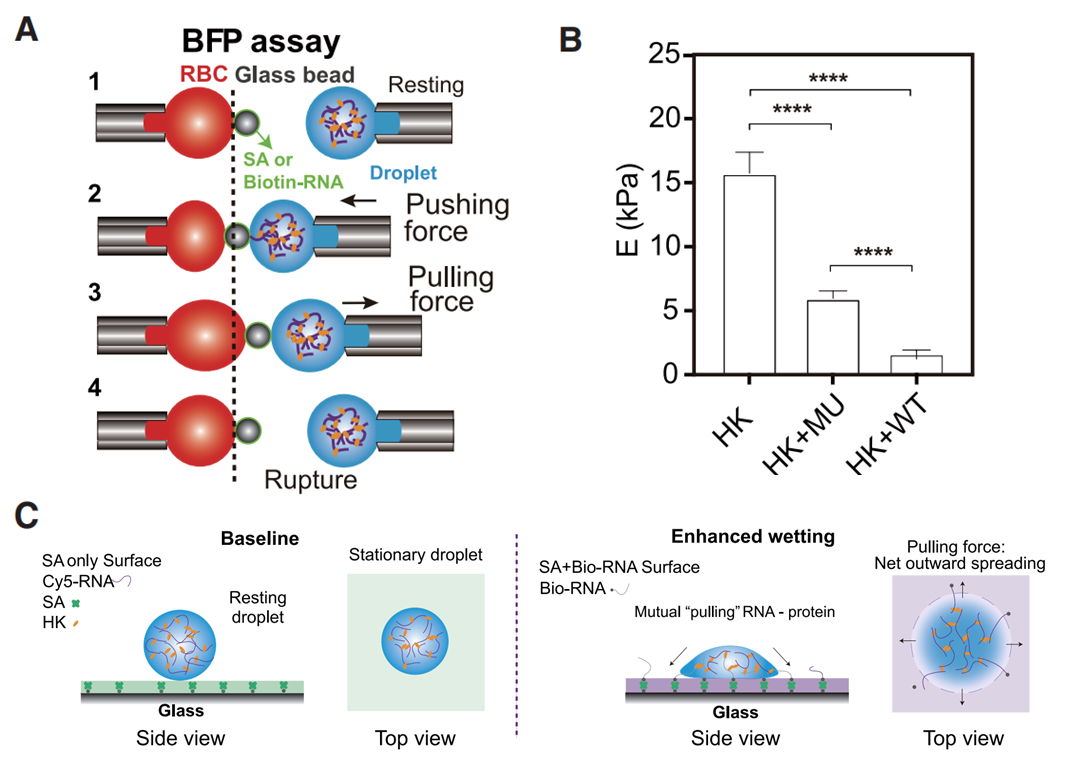
图4. RepB可以增加 HNRNPK 凝聚体的可变形性且二者之间存在相互吸引
体内功能验证与三维结构重塑
为了在体内验证相分离的生理学意义,团队利用shRNA敲低及突变体回补实验,观察了其对Xist-HNRNPK共定位、组蛋白修饰以及染色体超结构的影响。结果显示,敲低HNRNPK后,抑制性组蛋白修饰显著减少(图5A);回补野生型HNRNPK后修饰水平恢复,且与Xist呈现良好的共定位;但若回补的是丧失相分离能力的突变型HNRNPK,不仅修饰无法恢复,其与Xist也无法实现有效的空间共定位(图5B,C)。最后,原位高通量染色体构象捕获(Hi-C)技术揭示:RepB或RGG突变导致相分离失败后,失活X染色体内部长距离的染色质“混合”被显著阻断,Xi无法塌缩形成紧密的单一超结构(Superstructure),而是维持着类似活跃染色体的松散构象(图5D)。
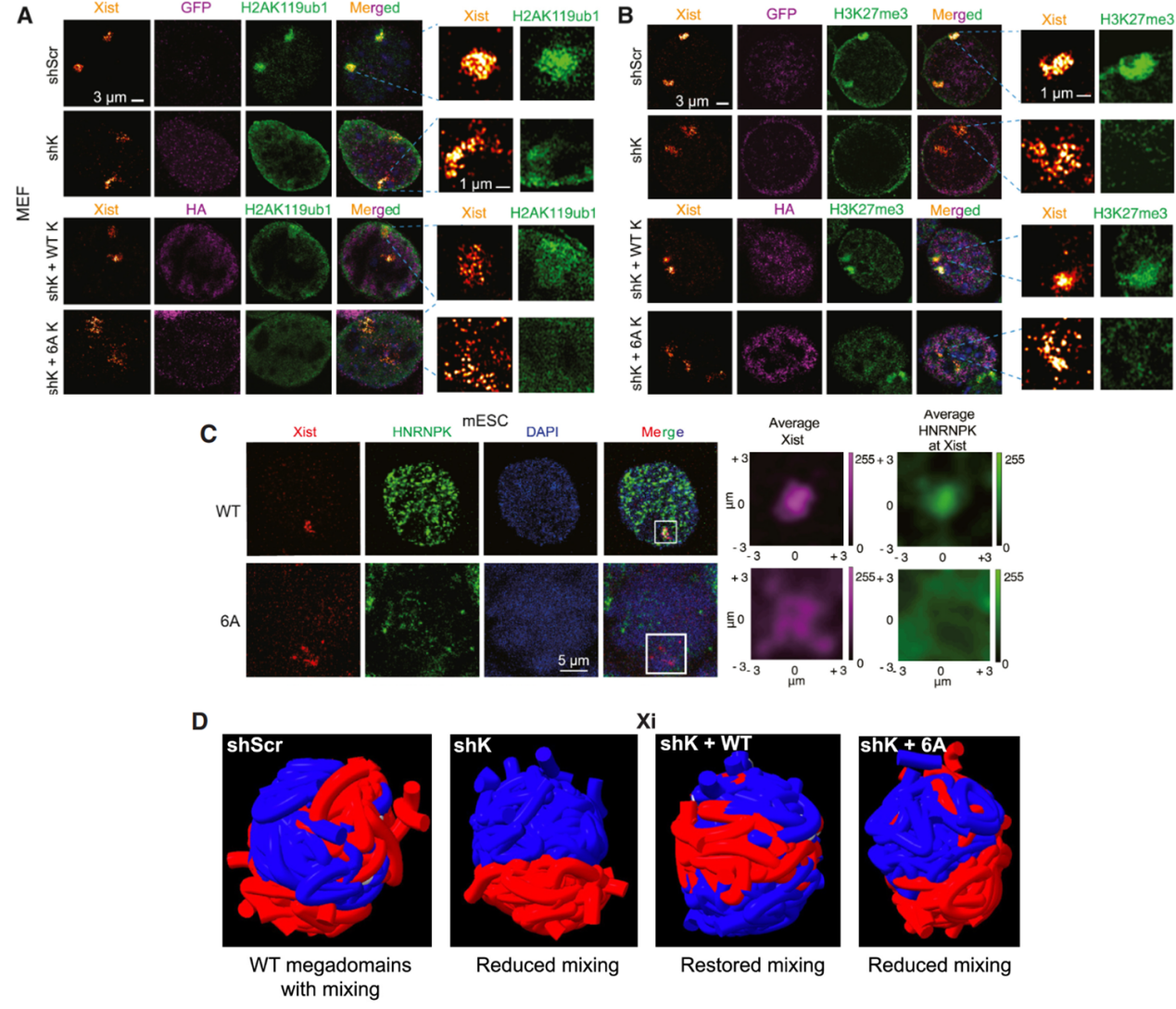
图5. HNRNPK相分离能力的缺失使Xi的转录抑制降低
综上所述,本研究揭示了一种由液-液相分离(LLPS)驱动的X染色体失活空间调控新机制。长链非编码RNA Xist与HNRNPK蛋白通过多价相互作用形成动态的液相凝聚体。Xist的加入不仅将表观遗传沉默因子高效招募、富集,更作为一种“大分子软化剂”,显著增加了凝聚体的可变形性与润湿性。这种特殊的物理性质使得包裹着沉默因子的“液相薄膜”能够紧密贴合并沿着染色体表面蔓延,不仅完美解答了Xist限制自身反式扩散的生物物理难题,也为失活X染色体三维超结构的力学塌缩与全基因组沉默提供了核心驱动力。
参考文献
1. Ding M, et al. Cell. 2025.
2. Brown CJ, et al. Nature. 1991.
3. Feric M, et al. Cell. 2016.